
 English
English
 French
French
Predictive factors of « severe OSA » status in patients with obstructive sleep apnea syndrome in Sub-Saharan Africa
Facteurs prédictifs du statut “SAOS sévère” au cours du syndrome d’apnée obstructif du sommeil en Afrique noire
Ulrich Davy KOMBILA1,2,3, Nicole BIVIGOU IDYATHA2, Price Léhonnore ANDJUMA4, Sephora TSIOUKAKA2, Jessica BOUANGA MAKAYA4, Jean Bruno BOGUIKOULA3
1Service de Médecine Interne, CHU de Libreville, Libreville, Gabon ;
2Service de Pneumologie, Institut des Maladies Infectieuses, PDG, Libreville, Gabon ;
3Faculté de Médecine de Libreville, Université des Sciences de la Santé, Libreville, Gabon;
4Service de Médecine Interne, HIA d’Akanda, Libreville, Gabon.
Corresponding author: Ulrich Davy KOMBILA. Service de Médecine Interne, CHU Libreville, Libreville - Gabon
Email: ulrichdavyk@gmail.com.
ABSTRACT
Introduction. – Undiagnosed or untreated sleep apnea syndrome induces different consequences. In addition, knowledge of the predictive factors of severity is necessary to target groups at risk of severity that can benefit from early diagnosis. The aim of this study was to identify the risk factors for severe OSA in patients with OSA.
Method. – This was a descriptive cohort study, with an analytical aim and retrospective data collection of patients with OSA. It is comparative between 87 patients with severe OSA and 92 patients with non-severe OSA.
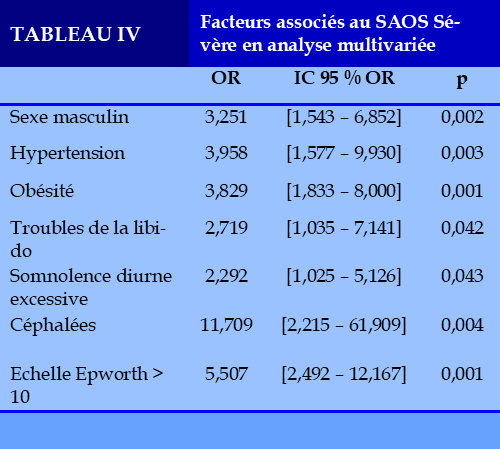
Results. – Out of 179 cases of OSA, the proportion of severe OSA is 48.6%. The average age was 51.36 (SD±12.2) years. The sex ratio was 2.25 (p=0.002). In logistic regression, the following signs were positively associated with the presence of severe OSAS: male gender (OR = 3.251 95% CI [1.543 – 6.852], p = 0.002), high blood pressure (OR = 3.958 95% CI [1.577 – 9.930], p = 0.003), obesity (OR = 3.829 95% CI [1.833 – 8.000], p = 0.001), libido disorders (OR = 2.719 95% CI [1.035 – 7.141], p = 0.042), excessive daytime sleepiness (OR = 2.292 95% CI [1.025 – 5.126], p = 0.043), headaches (OR = 11.709 95% CI [2.215 – 61.909], p=0.004) and an Epworth scale greater than 10 (OR=5.507 95% CI[2.492 – 12.167], p=0.001).
Conclusion. – Knowledge of the risk factors for severe OSAS should be brought to the attention of practitioners for early diagnosis to prevent progression to complications.
KEYWORDS: Sleep apnea; Severe OSA; Polygraphy; Predictive factors; Gabon.
RÉSUMÉ
Introduction. Le syndrome d’apnée du sommeil non diagnostiqué ou non traité induit différentes conséquences. De plus la connaissance des facteurs prédictifs de sévérité est nécessaire pour cibler les groupes à risque de sévérité pouvant bénéficier d’un diagnostic précoce. Le but de cette étude était d’identifier les facteurs de risque d’avoir un SAOS sévère chez les patients atteints de SAOS.
Méthode. Il s’agissait d’une étude de cohorte descriptive, à visée analytique à collecte de données rétrospective des patients porteurs d’un SAOS. Elle est comparative entre 87 patients atteints de SAOS sévère et 92 patients atteints de SAOS non sévère.
Résultats. Sur 179 cas de SAOS, la proportion de SAOS sévère était de 48,6%. La moyenne d’âge était de 51,36 (DS±12,2) ans. Le sex-ratio à 2,25 (p=0,002). En régression logistique, les signes suivants étaient positivement associés à la présence d’un SAOS sévère : le sexe masculin (OR = 3,251 IC95%[1,543 – 6,852], p=0,002), l’hypertension artérielle (OR = 3,958 IC95% [1,577 – 9,930], p=0,003), l’obésité (OR=3,829 IC95%[1,833 – 8,000], p=0,001), les troubles de la libido (OR=2,719 IC95% [1,035 – 7,141], p=0,042), la somnolence diurne excessive (OR=2,292 IC95%[1,025 – 5,126], p=0,043), les céphalées (OR=11,709 IC95%[2,215 – 61,909], p=0,004) et une échelle d’Epworth supérieure à 10 (OR=5,507 IC95%[2,492 – 12,167], p=0,001).
Conclusion. La connaissance des facteurs de risque du SAOS sévère doit être porter à la connaissance des praticiens pour un diagnostic précoce afin de prévenir l’évolution vers les complications.
MOTS CLÉS: Apnée du sommeil; SAOS sévère; Polygraphie; Facteurs prédictifs; Gabon.
INTRODUCTION
Le syndrome d’apnée hypopnée obstructif du sommeil (SAOS), malgré ses facteurs de risque cardiovasculaire et accidentel important, qui en font toute la gravité [1], demeure une pathologie méconnue et sous diagnostiquée en Afrique subsaharienne [2]. Parmi les raisons pouvant expliquer le sous diagnostic, on peut citer sa méconnaissance par la population générale et les médecins généralistes qui sont en première ligne dans le diagnostic indispensable de la maladie et l’insuffisance du plateau technique permettant l’enregistrement polysomnographique. La persistance de la tuberculose depuis l’avènement de l’infection à VIH, ainsi que la précarité sociale des populations occultent ce fléau silencieux pourtant associé à plusieurs autres pathologies chroniques [3]. Le SAOS a été individualisé dans les années 1970, depuis cette date sa prévalence ne cesse d’augmenter avec l’âge et concerne 4% des hommes et 2% des femmes [4, 5]. Il est indépendamment associé, à des pathologies responsables d’une morbidité et d’une mortalité cardiovasculaires accrue, notamment l’hypertension artérielle, l’insuffisance coronarienne, les accidents vasculaires cérébraux et le diabète de type 2 [6]. La fréquence élevée du SAOS, l’importance des pathologies associées, son impact sur la qualité de vie des patients en font donc un problème majeur de santé publique justifiant une bonne connaissance de cette pathologie afin d’optimiser la prise en charge diagnostique et thérapeutique. Afin d’élaborer de meilleures stratégies de dépistage et de traitement du SAOS, il est important d’identifier les facteurs de risque du SAOS. Les facteurs déterminants du SAOS sévère ont été très peu abordés dans les pays en développement. Nous formulons l’hypothèse selon laquelle qu’il existe des facteurs prédictifs de SAOS sévère chez les patients atteints de SAOS qu’il faudrait identifier pour une optimisation des actions de prévention. Dans ce contexte, ce travail se propose d’identifier les facteurs prédictifs de SAOS sévère auprès des patients atteints de SAOS.
MÉTHODES
Lieu et type d’étude
Il s’agit d’une étude de cohorte descriptive à collecte de données rétrospective de janvier 2020 à décembre 2024 à l’unité des maladies respiratoires du service de médecine interne du CHU de Libreville à partir des registres de consultation spécialisée des maladies respiratoires. La polygraphie ventilatoire nocturne a été réalisé à domicile avec un polygraphe d’un cabinet médical privé.
Critères de sélection
Les patients inclus ont tous un syndrome d’apnée obstructif du sommeil selon les critères A ou B et C de la Société de pneumologie de langue française (SPLF) et de l’Académie Américaine de Médecine du Sommeil (AASM) [7]. Ils sont âgés d’au moins 20 ans, quel que soit le sexe. Nous n’avons pas inclus les dossiers des patients qui présentaient les manifestations cliniques du SAOS, et qui n’avaient pas réalisé de polygraphie ventilatoire. Les patients souffrant des troubles du sommeil non lié à la respiration, les troubles mentaux ou psychiatriques ont été également exclus. Diagnostic du SAHOS L’HIA OBO ne possède pas de laboratoire de sommeil. En revanche, il existe en son sein deux appareils de polygraphie ventilatoire. Tous nos patients ont bénéficié d´une polygraphie ventilatoire durant une nuit d´hospitalisation dans une chambre ordinaire à un lit. Le polygraphe utilisé était soit de type CID Lx (PneaVox), soit le Nox T3 (version 1.1, Nox Medical ehf, Island). Le système relevait six signaux (flux nasal mesuré par le capteur correspondant à une lunette nasale, mouvements thoraciques et abdominaux (RIP) pour relever les efforts respiratoires, oxymétrie pour relever les désaturations nocturnes, fréquence cardiaque, position corporelle et activité). Le score des évènements a été réalisé selon les dernières recommandations de l'AASM. Le diagnostic du SAHOS a été retenu devant les signes clinique évocateurs selon les critères A ou B et C de la SPLF et un index d’apnées – hypopnées ([IAH]) supérieur ou égale à 5 / heure de sommeil. L’évaluation de la sévérité du SAHOS s’est basée sur l’IAH du sommeil par heure définissant ainsi trois stades de sévérité polygraphiques : SAHOS léger avec un [IAH] entre 5 à 15 par heure, le SAHOS modéré avec un [IAH] entre 15 à 30 par heure et le SAHOS sévère avec [IAH] supérieur ou égal à 30 par heure [8,9].
Au terme du dépouillement des dossiers, les patients ont été répartis en deux groupes pour les raisons d’étude : le groupe des patients au statut « SAHOS sévère » défini par un IAH supérieur ou égal à 30/heure de sommeil. Le groupe des témoins était des patients au statut « SAOS non sévère » défini par un IAH était inférieur à 30 par heure de sommeil.
Définitions opérationnelles des évènements respiratoires [7,9, 10].
Paramètres d’étude
Les paramètres suivants ont été recueillis : les paramètres sociodémographiques et anthropométriques (âge, genre, index de masse corporel), les comorbidités cardiovasculaires (hypertension artérielle, insuffisance cardiaque), métaboliques (diabète), et neuro-vasculaires (accident vasculaire cérébrale), les caractéristiques cliniques (ronflement, sensations de suffocation, insomnie, troubles de la libido, somnolence diurne excessive évaluée par le score d’Epworth, trouble de la mémoire, nycturie, asthénie, céphalées, irritabilité) et les paramètres polygraphiques ([IAH]).
Recueil et analyse des données
Les données ont été saisies sur une fiche de recueil (un seul enquêteur) comportant les variables d’intérêt renseignées à partir des registres des consultations et des dossiers des malades, transférées sur un fichier Excel. L’analyse a été rendue possible grâce au Logiciel SPSS version 25 (IBM Statistics). Les statistiques descriptives usuelles (moyenne, écart type (±ET), proportion, intervalle interquartile [IQR]) ont été utilisées pour présenter la synthèse de nos résultats. L’analyse des données était comparative entre le SAOS sévère (IAH ≥ 30/heure) et le SAOS non sévère (IAH < 30/heure). Les moyennes ± écart-types des variables qualitatives ont été comparées avec le test Anova. Le test de Khi2 de Pearson et le test de Fisher Exact en fonction des effectifs des sous-groupes ont été utilisés pour comparer les proportions des variables qualitatives en tableaux croisés. Les variables qualitatives avec des variations significatives entre le SAOS sévère (IAH≥30/heure) et le SAOS non sévère (IAH <30/heure) ont été intégrées dans le modèle de régression logistique pour une analyse multivariée. La valeur p<0,05 était considérée significative RESULTATS
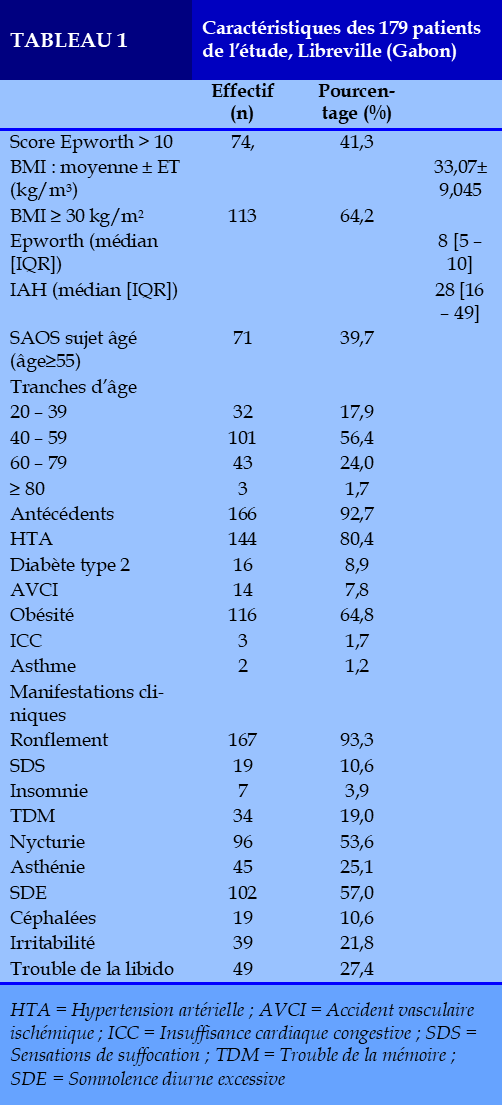
Caractéristiques générales de la population
L’étude a porté sur 179 cas de SAOS dont les caractéristiques sont présentées dans le (Tableau 1). La tranche d’âge de 40 à 59 ans représentait 56,4% (n=101) des patients. Cet effectif est composé de 124 sujets de sexe masculin et 55 sujets de sexe féminin, soit un sex-ratio homme / femme (sex-ratio H/F) de 2,25. La moyenne (±ET) d’âge était de 51,36 ans avec un écart type de 12,231. Les extrêmes d’âge étaient de 20 et 91 ans. La médiane (intervalle interquartile) d’âge est de 52 (42 – 60) ans. L’indice de masse corporelle moyen (±ET) était de 34,24 ± 9,5 kg/m2 chez les femmes et de 32,56 ± 8,8 kg/m2 chez les hommes (p=0,285). L’examen clinique retrouve une obésité dans 64,8% (n=116). Il s’agit d’une obésité modérée, sévère et morbide respectivement dans 30,5% (n=54), 20,3% (n=36) et 13,6% (n=24). L’étude des caractéristiques polygraphiques des patients révèle que 87 patients (48,6%) avaient un SAOS sévère et 92 sujets (51,4%) un SAOS non sévère. Seuls 25,1% (n=45) ont pu bénéficier d’un traitement par chambre à pression positive.
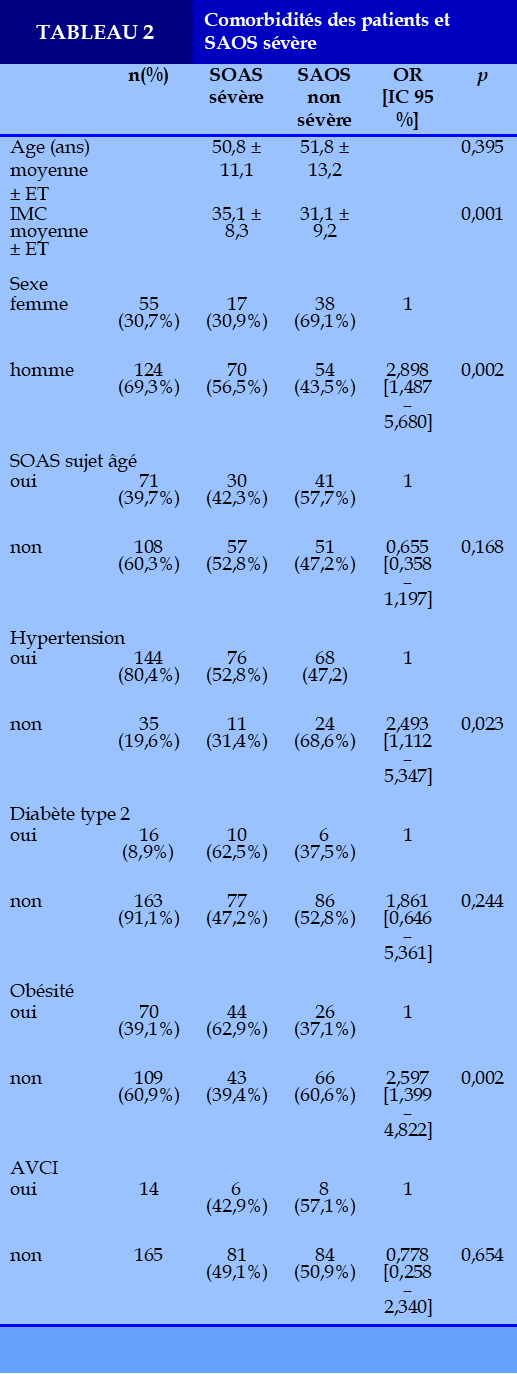
Comorbidités et statut « SAOS sévère »
La moyenne d’âge était superposable dans les deux groupes : 50,8 ans pour les patients avec SAOS sévère (IAH ≥ 30/heure) et 51,8 ans pour les patients avec SAOS non sévère (IAH < 30/heure) (p=0,395). L’indice de masse corporelle était plus important chez les patients avec SAOS sévère :35,1 kg/m2 contre 31,1 kg/m2 (p = 0,001). Le sex-ratio (H/F) était de 4,11 et 1,42 respectivement au sein des patients avec SAOS sévère et SAOS non sévère (OR = 2,898 [1,487 – 5,680], p=0,002). La proportion des hommes et femmes atteints respectivement de SAOS sévère et non sévère était de 56,5% et 30,9% (OR = 2,898 [1,487 – 5,680] p = 0,002). La fréquence de l’hypertension artérielle avec SAOS sévère était de 52,8% contre 47,2% pour le SAOS non sévère (OR=2,493 IC95% [1,112–5,347], p=0,023). L’obésité était plus fréquente en cas de SAOS sévère dans 62,9% contre 37,1% en cas de SAOS non sévère (OR=2,597 IC95% [1,399 – 4,822], p=0,002). L’incidence du SAOS sévère n’est pas liée à l’âge, au diabète de type 2, et l’accident vasculaire ischémique (Tableau 2).
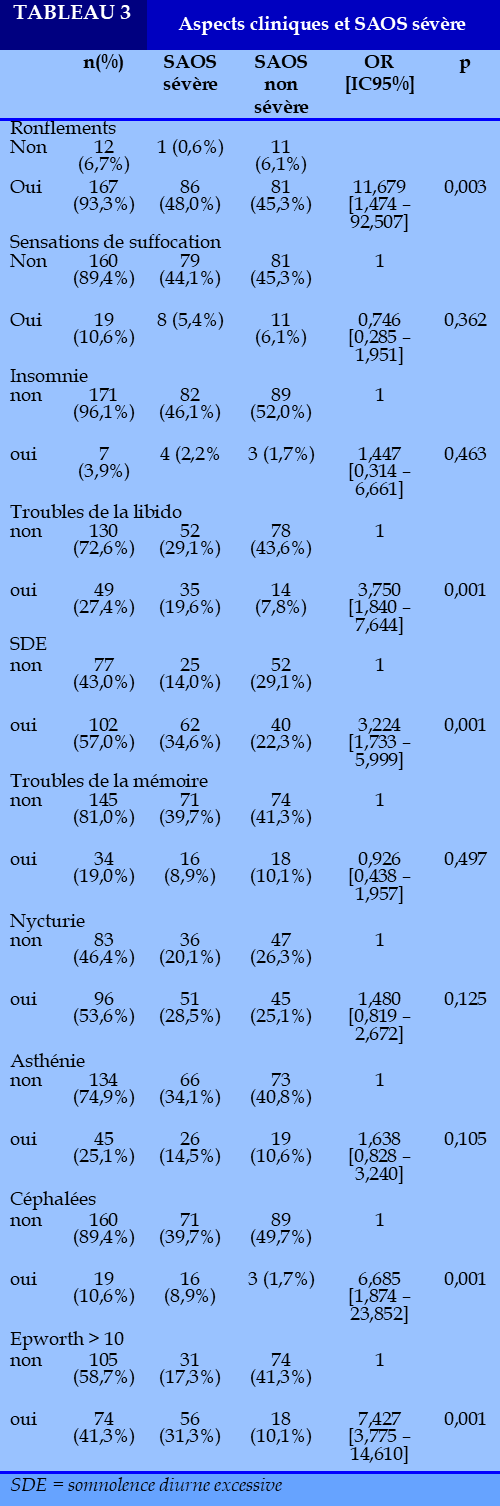
Signes cliniques et statut « SAOS sévère »
En cas de ronflement, 48,0% des patients avaient un SAOS sévère contre 0,6% en l’absence de ronflement (OR=11,679, IC95% [1,474 – 92,507], p=0,003). Nous avons noté 19,6% des troubles de la libido chez les patients avec SAOS sévère contre 7,8% avec SAOS non sévère (OR=3,750 IC95% [1,840 – 7,644], p=0,001). En cas de somnolence diurne excessive la proportion des SAOS sévère était de 34,6% contre 10,4% dans le cas contraire (OR=3,224 IC95% [1,733 – 5,999], p=0,001). La fréquence des céphalées était de 8,9% et 1,7% respectivement en cas de SAOS sévère et SAOS non sévère (OR=6,685 IC95% [1,874 – 23,852], p=0,001). Lorsque le score d’Epworth était supérieur à 10, chez 31,3% des patients avec un SAOS sévère contre 10,1% le cas contraire (OR=7,427 IC95% [3,775 – 14,610], p=0,001). Les autres manifestations cliniques (sensations de suffocation, insomnie, troubles de la mémoire, la nycturie, l’asthénie), sont rares et ne présentaient pas de lien avec le statut d’avoir un SAOS sévère (Tableau 3).
Facteurs indépendants de risque d’avoir un SAOS sévère
Les facteurs associés significativement au statut « SAOS sévère » en analyse univariée, ont été inclus dans le modèle de régression logistique binaire (Tableau 4). Les facteurs indépendants associés à une augmentation du risque d’avoir un SAOS sévère sont
DISCUSSION
Au terme de cette étude, l’interaction entre l’expression clinique du SAOS, les comorbidités d’une part et le statut « SAOS sévère », d’autre part est perceptible. Les patients de sexe masculin, hypertendu, obèse, avec les troubles de la libido, une somnolence diurne excessive, des céphalées et une Echelle d’Epworth supérieure à 10 ont plus de risque de SAOS sévère. Le SAOS sévère est important à étudier, car en plus du risque de complications métabolique et cardiovasculaire qu’il fait courir, il altère également la qualité de vie, les performances intellectuelles et professionnelles à cause de ses répercussions diurnes. Nous avons noté une prédominance masculine nette : 69,3% contre 30,7% ; soit un sex-ratio à 2,25/1. Cette prédominance masculine est retrouvée par d’autres auteurs [12, 13, 14]. Ailleurs cette prédominance n’est pas la règle : TOUIL et SAHNOUN en Tunisie [15, 16] et ZAGHBA au Maroc [1] retrouvent une prédominance féminine respectivement à 58,5%, 61,3%, 69%. Chez les personnes âgées, le SAHOS atteint de façon presque équivalente les deux sexes contrairement aux adultes d’âge moyen où il est deux fois plus fréquent chez l’homme [17]. Pour d’autres auteurs, les hommes ont un risque augmenté d’avoir un IAH supérieur ou égale à 15/h, avec des risques relatifs de 2,70 et 1,71 avant et après ajustement pour IMC, le périmètre cervical et le rapport taille/hanche, respectivement [18, 19]. Des hypothèses portant à la fois sur les différences hormonales ou anatomiques ont été proposées pour expliquer ces constatations épidémiologiques. Cette prévalence plus importante du SAHOS dans la population masculine est particulièrement vraie dans les cinq premières décennies. Au-delà de 50 ans, la prévalence du SAHOS chez les femmes augmente suggérant que la ménopause pourrait être un facteur de risque de SAHOS. La constatation d’une prévalence plus faible de SAHOS chez les femmes recevant un traitement hormonal substitutif que les femmes non substituées constituent un argument supplémentaire en faveur de cette hypothèse hormonale [18]. Le taux de prévalence du SAHOS sévère dans la présente étude (48,6%) semble comparable voire inférieure à celle retrouvée en consultation de sommeil chez les patients suspects de SAHOS dans les études en Asie du Sud-Est et certaines études d’Afrique subsaharienne. TRAN THI DIEM, rapporte un taux de prévalence de SAOS sévère de 86,7% au Viêtnam, chez les patients obèses [20]. NTIMA NSIEMI, rapporte 31,8% de SAOS sévère à Kinshasa [21]. ADJOH, rapporte un taux de SAOS sévère de 43,3% et 21,4% respectivement chez les hommes et les femmes au Benin [22]. La proportion du SAHOS sévère dans notre étude est importante en dépit de la gravité de cette affection. La forte prévalence du SAHOS sévère devrait stimuler le développement des politiques de santé publique afin de prévenir et traiter les complications liées à cette affection. L’obésité, définie par un indice de masse corporelle (IMC) supérieur à 30 kg/m2, est un facteur de développement d’un SAHOS [5]. La moyenne de l’IMC retrouvé dans l’étude était 35,1 kg/m2 dans le SAHOS sévère. L’IMC était corrélé positivement au SAHOS sévère. L’obésité est caractérisée par une infiltration des tissus mous par du tissu adipeux. Ceci est également vrai concernant les tissus mous oropharyngés mais également de la langue. C’est donc la principale cause d’obstruction des VAS puisque cette infiltration de tissu adipeux réduit directement le calibre pharyngé. Une adiposité viscérale peut également favoriser l’apparition d’apnées obstructives [3, 23]. D’autre part une compression abdominale par du tissu adipeux favorise la collapsibilité des VAS bien que les mécanismes précis soient difficiles à déterminer avec certitude [23]. La sévérité de la somnolence n’est pas toujours liée celle de l’IAH et celle du SAHOS n’est donc pas toujours corrélée ni à ses symptômes, ni à ses complications [24]. Dans l’étude les facteurs de risque corrélé à la sévérité du SAHOS étaient la somnolence diurne excessive, le score d’Epworth, l’hypertension artérielle, les troubles de la libido. Peu d’études en Afrique subsaharienne se sont intéressées aux facteurs de risque de sévérité du SAHOS. Les facteurs de risque de SAOS ont été décrits dans les pays développés. Le SAHOS est associé anatomiquement à un collapsus répété plus ou moins complet des voies aérodigestives supérieures. Ces épisodes d’apnées et d’hypopnées peuvent alors entraîner des conséquences ventilatoires dont une hypoxémie ou entraîner des répercussions sur la qualité du sommeil dont des micro-éveils [24]. Le lien de causalité est établi de façon formelle avec l’hypertension artérielle. En effet, la prévalence de l’HTA est plus élevée chez les patients apnéiques, et ceci indépendamment de facteurs habituellement retrouvés favorisant l’HTA tels que les paramètres anthropométriques, la consommation d’alcool et le tabagisme. Il s’agit d’une HTA à prédominance diastolique, avec un profil classiquement non dipper [19,25]. La pression artérielle (PA) s’abaisse au début de chaque apnée puis augmente progressivement jusqu’à un pic hypertensif survenant au moment de la reprise ventilatoire, la PA systolique pouvant s’accroître de 15 à 80 mmHg lors d’un micro-éveil cortical. Ces variations de PA surviennent sous l’influence de 4 stimulus : la désaturation en O2, l’élévation de la PaCO2, l’augmentation de l’effort respiratoire et le micro-éveil de fin d’apnée. Tous ces stimulus, particulièrement la désaturation, sont à l’origine d’une stimulation sympathique. La reprise respiratoire liée à un éveil ne se maintient pas longtemps, une nouvelle apnée apparaissant dès que le sujet se rendort. La succession de ces apnées aboutit à une fragmentation du sommeil qui perd son architecture normale [25,26]. D’où les recommandations majeures du 7ème rapport de la « Joint National Committee, Boston, USA » à l’égard des patients hypertendus avec un indice de masse corporelle au-dessus de 27 kg/m2 et qui exige qu’ils soient systématiquement examinés pour écarter toute implication du syndrome SAOS [27]. Les conséquences neurocognitives du SAHOS sont dominées par la somnolence diurne excessive qui est accompagnée de perturbations de la qualité de vie et des troubles cognitifs. L’échelle d’Epworth est très largement utilisée pour quantifier la somnolence diurne dans population. Le fait que plusieurs items de ce score, à savoir les questions relatives à la lecture, à la conduite automobile et aussi à la somnolence postprandiale de midi, ne sont pas applicables ou adaptés à notre population d’étude. Ceci montre le biais que pourrait créer l’échelle de somnolence d’Epworth dans le dépistage clinique du syndrome d’apnée obstructive du sommeil dans le contexte africain [28].
CONCLUSION
La présence de la somnolence diurne excessive, le score d’Epworth, l’hypertension artérielle, les troubles de la libido étaient associés à un risque de sévérité du SAHOS sévère. Le défi de la lutte contre les complications liées au syndrome d’apnée obstructif du sommeil doit passer par l’enregistrement polygraphique nocturne à tous les patients présentant au moins un des facteurs prédictifs de SAOS sévère suscités.
REFERENCES
| 1. Zaghba N, Chaanoun K, Benjelloun H, Yassine N. Profil épidémiologique, clinique et évolutif du syndrome d’apnées obstructives du sommeil au Service des Maladies Respiratoires du CHU Ibn Rochd de Casablanca. J Func Vent Pulm 2021 ; 36(12) : 47 – 55. |
| 2. Ba F, Sène M, El Hadji Makhtar B.A., et al. Syndrome d’apnée hypopnée obstructif du sommeil en Afrique Sub-saharienne : une revue de la littérature. Med Sommeil 2020 ; 17 : 169 – 176. |
| 3. Kashongwe IM, Ntumba Kayembe JM, Kashongwe ZM, et al. Syndrome d’Apnées hypopnées obstructives du sommeil (SAOS) en Afrique subsaharienne : revue de la littérature, état de lieux et perspectives. Ann. Afr. Med., 2019 ; 12(2) : e3257 – e3261. |
| 4. Rajaoarifetra J, Palot A, Tissier Ducamps D et al. Le syndrome d’apnées obstructives du sommeil n’est pas mauvais que pour le cœur. Rev Mal Respir 2018 ; 35 : 562 – 566. |
| 5. Frija-Orvoën E. Syndrome d’apnées obstructives du sommeil : complications métaboliques. Rev Mal Respir 2016 ; 33 : 474 – 483. |
| 6. Meslier N, Vol S, Balkau B et al. Prévalence des symptômes du syndrome d’apnées du sommeil. Etude dans une population française d’âge moyen. Rev Mal Respir 2007 ; 24 : 305 – 13. |
| 7. Satéia MJ. International Classification of Sleep Disorders-Third Edition. Chest 2014; 146: 1387 – 1394 |
| 8. Soori R, Baikunje N, D’sa I, Bhushan N, Nagabhushana B, Hosmane GB. Pitfalls of AHI system of severity grading in obstructive sleep apnoea. Sleep Sci 2022; 15: 285 – 288. |
| 9. Won L, Swamy N, Meir H. K, Babak M. Epidemiology of Obstructive Sleep Apnea: a Population-based Perspective. Expert Rev Respir Med. 2008; 2(3): 349–364. |
| 10. Medical Advisory Secretariat. Polysomnography in patients with obstructive sleep apnea: an evidence-based analysis. Ontario Health Technology Assessment Series 2006; 6(13). |
| 11. Johns MW. A new method for measuring day time sleepiness : the Epworth Sleepiness scale. Sleep 1991 ; 14 : 540 – 5. |
| 12. Agdokpessi G, Adohouannon G, Wachinou AP, Awanou B, Fiogbe A, Ade S, Gninafon M. Facteurs associés au SaHOS modéré à sévère en Afrique noire : données préliminaires à Cotonou, Bénin (Afrique de l’Ouest). Rev Mal Respir 2019 ; A70 ; AD07 : 120. https://doi.org/10.1016/j.rmr.2018.10.133. |
| 13. Goddaert C, Jender A, Zulfiqar AA. Syndrome d’apnées du sommeil : caractéristiques cliniques des patients atteints dans la population hospitalière de Château-Thierry. Rev Mal Respir 2019 ; 36 : 326 – 332. |
| 14. Duong-Quy S, Dang Thi Mai K, Tran Van N et al. Etude de la prévalence du syndrome d’apnées obstructives du sommeil au Vietnam. Rev Mal Respir 2018 ; 35 : 14 – 24. |
| 15. Touil I, Boudawara N, Bouchared S, Zaafouri A, Omrane A, Knani J, Boussoffara L. Evaluation de la capacité à l’effort des patients atteints d’un syndrome d’apnée obstructives du sommeil sévère. Rev Mal Respir 2019 ; 554 : A246. |
| 16. Shanoun I, Ouahchi Y, Mjid M, Snéne H, Toujeni S, Ben Salah N et al. Profil clinique et polygraphique de patients tunisiens porteurs d’un syndrome d’apnées obstructives du sommeil (SAOS). Rev Mal Respir 2015 ; 665 : A209. |
| 17. Ketata W, Feki W, Yangui I, Msaad S, Ayoub A. Le syndrome d’apnées obstructives du sommeil du sujet âgé. Rev Pneumol Respir 2014 ; 70(4) : 223 – 232. |
| 18. Trzepizur W, Gagnadoux F. Epidémiologie du syndrome d’apnées-hypopnées obstructives du sommeil. Rev Mal Respir 2014 ; 31 : 568 – 577. |
| 19. Escourrou P, Roisman GL. Epidémiologie du syndrome d’apnées-hypopnées obstructives du sommeil de l’adulte et ses complications. Med Som 2010 ; 7 : 119 – 128. |
| 20. Tran Thi Diem T, Nguyen Thi Doan T, Nguyen Huy D, Nguyen Hong D. Syndrome d’apnées obstructives du sommeil : première expérience à l’hôpital Pham Ngoc Thach - HCM ville. J Func Vent Pulm 2011 ; 5(2) : 1-94. |
| 21. Ntima Nsiemi AK, Kayembe JMN, Mbuila CN, Sokolo RM, Kubiluka J, Dilu F, Madaka C. Syndrome d’Apnées-Hypopnées Obstructives du Sommeil : Profil Clinique et Polygraphique des Patients à Kinshasa. Health Sci. Dis 2022 ; 23(7) : 45 – 51. |
| 22. Adjoh KS, Adambounou AS, Gbadamassi AG et al. Syndrome d’apnées obstructives durant le sommeil : Aspects épidémiolo giques, cliniques et paracliniques des premiers cas à Lomé. J Func Vent Pulm 2017 ; 24(8) : 10 – 17. |
| 23. Bironneau V,. Meurice J.C. Prise en charge thérapeutique du syndrome d’apnées obstructives du sommeil : vers une médecine personnalisée. Médecine du Sommeil 2019 ; 16 : 225 – 237. |
| 24. Jaffuel D, Charriot J, Jean R, Alagha K, Palot A, Bourdin A, Mallet J.P. Est-il si facile de faire le diagnostic d’un syndrome d’apnées obstructives du sommeil ? La Lettre du Pneumologue 2017 ; XX (3) : 210 – 215. |
| 25. Destors M, Tamisier R, Baguet J.-P, Levy P, Pepin J.-L. Morbidité cardiovasculaire associée au syndrome d’apnée obstructive du sommeil. Rev Mal Respir 2014 ; 31 : 375 – 85. |
| 26. Baguet J.-P, Pépin J.-L, Hammer L, Lévy P, Mallion J.-M. Conséquences cardiovasculaires du syndrome d’apnées obstructives du sommeil. Med Int 2003 ; 24 : 530 – 537. |
| 27. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr, et al. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension. 2003 : 42(6):1206–52. |
| 28. Azon Kouanou A, Agbodande KA1, Djiholissè TN, Missiho MSG, Sokadjo YM, Faladé AAG, Moussé L, Zannou DM. Syndrome d’apnées obstructives du sommeil chez les patients présentant une HTA à prédominance nocturne : prévalence et facteurs associés. Rev Afr Med Int 2021 : 8(2) : 55 – 62. |
FIGURES - TABLES
REFERENCES
| 1. Zaghba N, Chaanoun K, Benjelloun H, Yassine N. Profil épidémiologique, clinique et évolutif du syndrome d’apnées obstructives du sommeil au Service des Maladies Respiratoires du CHU Ibn Rochd de Casablanca. J Func Vent Pulm 2021 ; 36(12) : 47 – 55. |
| 2. Ba F, Sène M, El Hadji Makhtar B.A., et al. Syndrome d’apnée hypopnée obstructif du sommeil en Afrique Sub-saharienne : une revue de la littérature. Med Sommeil 2020 ; 17 : 169 – 176. |
| 3. Kashongwe IM, Ntumba Kayembe JM, Kashongwe ZM, et al. Syndrome d’Apnées hypopnées obstructives du sommeil (SAOS) en Afrique subsaharienne : revue de la littérature, état de lieux et perspectives. Ann. Afr. Med., 2019 ; 12(2) : e3257 – e3261. |
| 4. Rajaoarifetra J, Palot A, Tissier Ducamps D et al. Le syndrome d’apnées obstructives du sommeil n’est pas mauvais que pour le cœur. Rev Mal Respir 2018 ; 35 : 562 – 566. |
| 5. Frija-Orvoën E. Syndrome d’apnées obstructives du sommeil : complications métaboliques. Rev Mal Respir 2016 ; 33 : 474 – 483. |
| 6. Meslier N, Vol S, Balkau B et al. Prévalence des symptômes du syndrome d’apnées du sommeil. Etude dans une population française d’âge moyen. Rev Mal Respir 2007 ; 24 : 305 – 13. |
| 7. Satéia MJ. International Classification of Sleep Disorders-Third Edition. Chest 2014; 146: 1387 – 1394 |
| 8. Soori R, Baikunje N, D’sa I, Bhushan N, Nagabhushana B, Hosmane GB. Pitfalls of AHI system of severity grading in obstructive sleep apnoea. Sleep Sci 2022; 15: 285 – 288. |
| 9. Won L, Swamy N, Meir H. K, Babak M. Epidemiology of Obstructive Sleep Apnea: a Population-based Perspective. Expert Rev Respir Med. 2008; 2(3): 349–364. |
| 10. Medical Advisory Secretariat. Polysomnography in patients with obstructive sleep apnea: an evidence-based analysis. Ontario Health Technology Assessment Series 2006; 6(13). |
| 11. Johns MW. A new method for measuring day time sleepiness : the Epworth Sleepiness scale. Sleep 1991 ; 14 : 540 – 5. |
| 12. Agdokpessi G, Adohouannon G, Wachinou AP, Awanou B, Fiogbe A, Ade S, Gninafon M. Facteurs associés au SaHOS modéré à sévère en Afrique noire : données préliminaires à Cotonou, Bénin (Afrique de l’Ouest). Rev Mal Respir 2019 ; A70 ; AD07 : 120. https://doi.org/10.1016/j.rmr.2018.10.133. |
| 13. Goddaert C, Jender A, Zulfiqar AA. Syndrome d’apnées du sommeil : caractéristiques cliniques des patients atteints dans la population hospitalière de Château-Thierry. Rev Mal Respir 2019 ; 36 : 326 – 332. |
| 14. Duong-Quy S, Dang Thi Mai K, Tran Van N et al. Etude de la prévalence du syndrome d’apnées obstructives du sommeil au Vietnam. Rev Mal Respir 2018 ; 35 : 14 – 24. |
| 15. Touil I, Boudawara N, Bouchared S, Zaafouri A, Omrane A, Knani J, Boussoffara L. Evaluation de la capacité à l’effort des patients atteints d’un syndrome d’apnée obstructives du sommeil sévère. Rev Mal Respir 2019 ; 554 : A246. |
| 16. Shanoun I, Ouahchi Y, Mjid M, Snéne H, Toujeni S, Ben Salah N et al. Profil clinique et polygraphique de patients tunisiens porteurs d’un syndrome d’apnées obstructives du sommeil (SAOS). Rev Mal Respir 2015 ; 665 : A209. |
| 17. Ketata W, Feki W, Yangui I, Msaad S, Ayoub A. Le syndrome d’apnées obstructives du sommeil du sujet âgé. Rev Pneumol Respir 2014 ; 70(4) : 223 – 232. |
| 18. Trzepizur W, Gagnadoux F. Epidémiologie du syndrome d’apnées-hypopnées obstructives du sommeil. Rev Mal Respir 2014 ; 31 : 568 – 577. |
| 19. Escourrou P, Roisman GL. Epidémiologie du syndrome d’apnées-hypopnées obstructives du sommeil de l’adulte et ses complications. Med Som 2010 ; 7 : 119 – 128. |
| 20. Tran Thi Diem T, Nguyen Thi Doan T, Nguyen Huy D, Nguyen Hong D. Syndrome d’apnées obstructives du sommeil : première expérience à l’hôpital Pham Ngoc Thach - HCM ville. J Func Vent Pulm 2011 ; 5(2) : 1-94. |
| 21. Ntima Nsiemi AK, Kayembe JMN, Mbuila CN, Sokolo RM, Kubiluka J, Dilu F, Madaka C. Syndrome d’Apnées-Hypopnées Obstructives du Sommeil : Profil Clinique et Polygraphique des Patients à Kinshasa. Health Sci. Dis 2022 ; 23(7) : 45 – 51. |
| 22. Adjoh KS, Adambounou AS, Gbadamassi AG et al. Syndrome d’apnées obstructives durant le sommeil : Aspects épidémiolo giques, cliniques et paracliniques des premiers cas à Lomé. J Func Vent Pulm 2017 ; 24(8) : 10 – 17. |
| 23. Bironneau V,. Meurice J.C. Prise en charge thérapeutique du syndrome d’apnées obstructives du sommeil : vers une médecine personnalisée. Médecine du Sommeil 2019 ; 16 : 225 – 237. |
| 24. Jaffuel D, Charriot J, Jean R, Alagha K, Palot A, Bourdin A, Mallet J.P. Est-il si facile de faire le diagnostic d’un syndrome d’apnées obstructives du sommeil ? La Lettre du Pneumologue 2017 ; XX (3) : 210 – 215. |
| 25. Destors M, Tamisier R, Baguet J.-P, Levy P, Pepin J.-L. Morbidité cardiovasculaire associée au syndrome d’apnée obstructive du sommeil. Rev Mal Respir 2014 ; 31 : 375 – 85. |
| 26. Baguet J.-P, Pépin J.-L, Hammer L, Lévy P, Mallion J.-M. Conséquences cardiovasculaires du syndrome d’apnées obstructives du sommeil. Med Int 2003 ; 24 : 530 – 537. |
| 27. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr, et al. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension. 2003 : 42(6):1206–52. |
| 28. Azon Kouanou A, Agbodande KA1, Djiholissè TN, Missiho MSG, Sokadjo YM, Faladé AAG, Moussé L, Zannou DM. Syndrome d’apnées obstructives du sommeil chez les patients présentant une HTA à prédominance nocturne : prévalence et facteurs associés. Rev Afr Med Int 2021 : 8(2) : 55 – 62. |
ARTICLE INFO DOI: 10.12699/jfvpulm.17.51.2026.38
Conflict of Interest
Non
Date of manuscript receiving
10/9/2025
Date of publication after correction
25/11/2025
Article citation
Ulrich Davy KOMBILA, Nicole BIVIGOU IDYATHA, Price Léhonnore ANDJUMA, Sephora TSIOUKAKA, Jessica BOUANGA MAKAYA, Jean Bruno BOGUIKOULA. Predictive factors of « severe OSA » status in patients with obstructive sleep apnea syndrome in Sub-Saharan Africa. J Fran Vent PulmS 2026;51(17):44-50