
 English
English
 French
French
Severe COPD with frequent exacerbations and suspicion of overlap syndrome in a retired 64 years-old patient: A case report
BPCO sévère avec exacerbations fréquentes et suspicion de syndrome de chevauchement chez un patient retraité de 64 ans: Un cas clinique
Iris Hadadji1, Lucie Pellier, Julia Pessiglione1, Georgia Gesseau1, Tang-Thi-Thao Tram2,3, Nguyen-Tuan Anh2,3, Do Xuan Hai2, Bui Thi Kim Chi4, Cao Thi Hong Mai4, Pham Vu Thanh4, Nguyen Xuan Tao4, Victoire de Lastours1,5, Sy Duong-Quy1,2,3
1Faculté de Médecine. Université Paris Cité. Paris, France
2Centre de Recherche Biomédicale. Collège de Médecine de Lam Dong. Lam Dong, Vietnam
3La Société Vietnamienne de la Médecine du Sommeil. Lam Dong, Vietnam
4Service de Pneumologie. Hôpital Général de Lam Dong. Lam Dong, Vietnam
5Service de Médecine Interne. Hôpital Beaujon, AP-HP Nord. Clichy, France
Corresponding author: Sy Duong-Quy. Lam Dong Medical College. Penn State University. Paris Cite University
Email: sduongquy.jfvp@gmail.com
ABSTRACT
Background. Chronic Obstructive Pulmonary Disease (COPD) remains a leading cause of morbidity worldwide. Severe COPD with frequent exacerbations and insufficient follow-up poses major challenges, especially in resource-limited settings. The possible coexistence of obstructive sleep apnea (overlap syndrome) further worsens prognosis. Observation. We report the case of a 64-year-old retired military man with long-standing severe COPD diagnosed in 2015, under triple therapy and long-term oxygen therapy (2 L/min at home), who experienced frequent hospitalizations (every 1-3 months) for exacerbations. He presented with an acute worsening of dyspnea; biological tests showed moderate neutrophilic leukocytosis and mild hypokalemia, but no clear sign of infection. Physical exam revealed barrel chest, diminished vesicular murmur, bilateral tympany and bronchial rales. Treatment included systemic corticosteroids, bronchodilators, mucolytics, oxygen therapy and metabolic management. Because of severe disease, frequent exacerbations and persistent hypoxemia, overlap with undiagnosed obstructive sleep apnea (OSA) was suspected. Conclusion. This case underlines the critical need for systematic functional evaluation, optimized maintenance therapy, reassessment of oxygen requirements and screening for OSA in severe COPD patients with frequent exacerbations. A comprehensive, multidisciplinary and protocolized management can improve outcomes even in limited-resource settings.
KEYWORDS: COPD; Exacerbations; Overlap syndrome; Long-term oxygen therapy; OSA; Lam Dong General Hospital.
RÉSUMÉ
Contexte. La bronchopneumopathie chronique obstructive (BPCO) demeure l’une des principales causes de morbidité dans le monde. Les formes sévères, associées à des exacerbations fréquentes et à un suivi insuffisant, représentent un défi majeur, en particulier dans les contextes à ressources limitées. La coexistence possible d’un syndrome de chevauchement avec le syndrome d’apnées obstructives du sommeil (overlap syndrome) aggrave encore le pronostic. Observation. Nous rapportons le cas d’un homme de 64 ans, ancien militaire, atteint d’une BPCO sévère évoluant depuis 2015, traité par une triple thérapie inhalée et une oxygénothérapie de longue durée (2 L/min au domicile), présentant des hospitalisations répétées (environ tous les 1-3 mois) pour exacerbations. Il a consulté pour une majoration aiguë de la dyspnée. Le bilan biologique retrouvait une hyperleucocytose neutrophile modérée et une hypokaliémie légère, sans argument en faveur d’une infection active. L’examen clinique révélait un thorax en tonneau, une diminution du murmure vésiculaire, un tympanisme bilatéral et des râles bronchiques. Le traitement instauré comprenait des corticoïdes systémiques, des bronchodilatateurs, des mucolytiques, une oxygénothérapie et la prise en charge des comorbidités métaboliques. En raison de la sévérité de la maladie, des exacerbations répétées et de l’hypoxémie persistante, un syndrome de chevauchement avec un syndrome d’apnées obstructives du sommeil (SAOS) non diagnostiqué a été suspecté. Conclusion. Ce cas illustre la nécessité essentielle d’une évaluation fonctionnelle systématique, d’une optimisation du traitement de fond, d’une réévaluation des besoins en oxygène et d’un dépistage du SAOS chez les patients atteints de BPCO sévère avec exacerbations fréquentes. Une prise en charge globale, multidisciplinaire et protocolisée peut améliorer les résultats, même dans les environnements à ressources limitées.
MOTS CLÉS: BPCO; Exacerbation; Syndrome de chevauchement; OLD; SAOS; Hôpital Général de Lam Dong.
INTRODUCTION
La Broncho-Pneumopathie Chronique Obstructive (BPCO) constitue un problème de santé publique majeur, caractérisée par la limitation persistante du débit expiratoire et des exacerbations fréquentes. Selon les données récentes, plus de 250 millions de personnes vivent avec une BPCO dans le monde, et cette maladie est responsable d’une mortalité élevée [1].
Cependant, dans un contexte de suivi thérapeutique irrégulier et de comorbidités associées telles que les complications cardiovasculaires et métaboliques ou encore l’hypoxémie chronique, la BPCO peut avoir un phénotype sévère, difficile à contrôler, avec un risque accru de complications comme des hospitalisations à répétition, le déclin fonctionnel respiratoire, ou le haut risque de mortalité [2,3].
Un facteur souvent sous-estimé est la coexistence possible d’un syndrome d’apnées obstructives du sommeil (SAOS), formant un « syndrome de chevauchement », qui aggrave l’hypoxémie nocturne, la fragmentation du sommeil et la charge inflammatoire. L’absence de dépistage du SAOS chez les patients BPCO sévères constitue un manquement important à la prise en charge optimale [4,5].
Nous présentons ici le cas d’un patient BPCO sévère avec exacerbations fréquentes, suivi irrégulier, oxygénothérapie à domicile, dont l’aggravation récente met en lumière les lacunes du suivi et l’impérieuse nécessité d’un diagnostic fonctionnel complet et d’un dépistage d’OSA.
OBSERVATION
Le patient est un homme de 64 ans, ancien militaire à la retraite, vivant en zone rurale. Son histoire tabagique est particulièrement marquée : il a fumé en moyenne deux paquets de cigarettes par jour depuis l’âge de 20 ans jusqu’à 61 ans, soit un total de 82 paquet-années. Il est sevré du tabac depuis trois ans. La BPCO a été diagnostiquée en 2015, mais son suivi pneumologique est resté très irrégulier. Les dernières épreuves fonctionnelles respiratoires (EFR) et gazométries artérielles datent de plus de cinq ans, ce qui rend difficile l’évaluation actuelle de la sévérité de sa pathologie.
Son traitement de fond repose sur une trithérapie inhalée quotidienne: Trelegy® (Fluticasone, Umeclidinium, Vilanterol) administré le matin, associée à Seretide® matin et soir. Le patient utilise par ailleurs des bronchodilatateurs de secours, dont Berodual® et Banbuterol®, ainsi qu’une oxygénothérapie de longue durée à 2 L/min 24 heures sur 24, prescrite en raison d’une dyspnée sévère au moindre effort (mMRC 4). Malgré ce traitement relativement intensif, il présente des exacerbations fréquentes nécessitant en moyenne une hospitalisation tous les trois à quatre mois.
Le patient présente également des comorbidités méta boliques: un diabète de type 2 diagnostiqué sept ans auparavant, traité par gliclazide et insuline retard (10 UI matin et soir), ainsi qu’une hypertension artérielle sous losartan 50 mg/j. Il ne rapporte aucune allergie connue et ne se souvient plus de ses derniers vaccins, notamment pneumocoque et grippe.
L’évolution
Deux semaines avant son admission actuelle, le patient avait déjà été hospitalisé pour une exacerbation de sa BPCO, sans fièvre ni détresse respiratoire aiguë. À sa sortie, une nouvelle aggravation progressive de la dyspnée l’a conduit aux urgences le 29 novembre 2025. À l’admission, les constantes vitales montraient une fréquence cardiaque de 98 bpm, une pression artérielle de 150/100 mmHg, une fréquence respiratoire de 22 cycles/minute et une saturation en oxygène à 95 % sous 2 L/min d’oxygène. Il était afébrile (37 °C) et pesait 55 kg.
Le bilan biologique initial révélait une hyperleucocytose modérée dominée par les polynucléaires neutrophiles (12,56 G/L dont PNN 10,38 G/L), associée à une lymphopénie (0,85 G/L) et une hypokaliémie (K+ 3,3 mmol/L). La fonction rénale et les enzymes hépatiques étaient normales. La CRP était faiblement élevée (2 mg/dL), sans argument fort pour une infection bactérienne active. Aucun examen radiologique, gaz du sang artériel ou EFR récents n’étaient disponibles.
Aux urgences, un bronchodilatateur de courte durée d’action (terbutaline) a été administré, puis le patient a été transféré en service de pneumologie. Le traitement instauré reposait sur Solumédrol 40 mg/j, Vinterlin® 0,8 mg/j, Banbuterol 10 mg/j, Salbutamol 16 mg/j en BDCA, acétylcystéine 40 mg/j, oméprazole 40 mg/j, Losartan 50 mg/j ainsi qu’un ajustement de l’insulinothérapie.
À l’examen clinique du jour, le patient est calme, orienté, eupnéique sous 2 à 3 L/min d’oxygène avec une SpO₂ de 95 %. Le murmure vésiculaire est globalement diminué aux deux champs pulmonaires, avec des râles bronchiques à mi-champ droit. La percussion montre un thorax tympanique avec morphotype en tonneau. Les bruits cardiaques sont réguliers, les pouls périphériques perçus et il n’existe aucun signe clinique d’insuffisance cardiaque. L’examen abdominal est strictement normal. Le score de symptôme de la BPCO (CAT) est de 32/40.
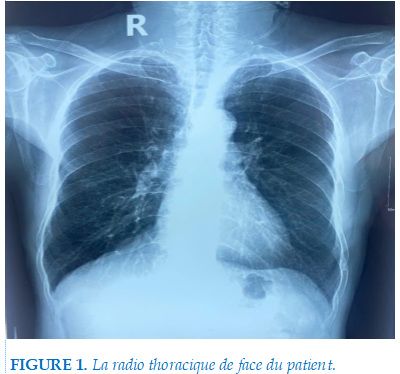
Le patient rapporte des épisodes de réveils nocturnes avec sensation d’étouffement, un ronflement ancien et intense, ainsi qu’une somnolence importante pendant la journée, confirmée par un score d’Epworth à 14/28. Le dépistage clinique par STOP-Bang a retrouvé 4 critères positifs, classant le patient dans la catégorie de risque élevé pour SAOS. Par ailleurs, l’examen physique ORL objectivait un Mallampati classe IV. Lors de l’hospitalisation, le patient a fait une radiographie thoracique qui ne montre pas d’anomalie majeure en dehors d’une dis tension thoracique: élargissement des espaces intercostaux et horizontalisation des côtes, et quelques plages d’emphysèmes (Figure 1). Les gaz du sang réalisées au même jour de la radio thoracique sous oxygène de 3L/min montrait la PaO2= 124 mmHg, la PaCO2=33 mmHg, le pH=7,42, l’HCO3-=22,4 mEq/L.
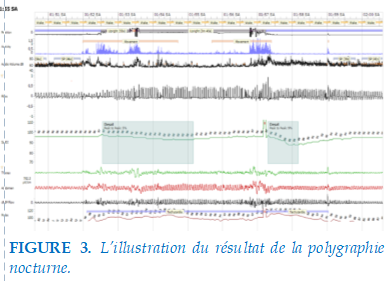
Le patient a eu la polygraphie intégrée de l’actigraphie (NOX-T3S; Figure 2). Les résultats de la polygraphie nocturne sous oxygène 1L/min sont les suivants: l’index d’apnées – hypopnées (IAH) est de 8 événements/heure, associé à des mouvements thoraco-abdominaux d’effort pendant le sommeil; SpO₂ moyenne: 94,8 %; SpO₂ minimale: 87,0 %; ronflement: pourcentage de ronflement: 36,2 %; intensité sonore moyenne du ronflement: 63 dBc; sommeil de mauvaise efficacité (50 %), avec une prédominance du sommeil léger (Figure 3).
DISCUSSION
Ce cas illustre une forme sévère de BPCO à phénotype « exacerbeur fréquent », associée à des comorbidités métaboliques et à un syndrome d’apnées du sommeil (SAOS) suspecté puis confirmé par polygraphie nocturne. La fréquence élevée des exacerbations, le recours à l’oxygénothérapie de longue durée, l’indication de la réhabilitation respiratoire ainsi que l’absence de couverture vaccinale constituent des éléments clés de la prise en charge globale (Figure 4).
Fréquence des exacerbations de la BPCO: rôle des infections, de la fatigue et des apnées nocturnes
Le patient présente des exacerbations très fréquentes, avec une hospitalisation tous les trois à quatre mois, ce qui signe une BPCO sévère et instable. Les exacerbations sont le plus souvent déclenchées par des infections respiratoires, virales ou bactériennes, même en l’absence de syndrome infectieux franc, comme le suggère ici la CRP faiblement élevée. La fatigue chronique, liée à l’hypoxémie, à la dénutrition probable (IMC bas) et au mauvais sommeil, constitue également un facteur aggravant majeur [5-9].
La présence d’un SAOS léger (IAH à 8/h), associé à une mauvaise efficacité du sommeil (50 %), à une somnolence diurne importante et à une hypoxémie nocturne, participe probablement à la fréquence des exacerbations. Le chevauchement BPCO–SAOS (« overlap syndrome ») est reconnu comme un facteur de mauvais pronostic, augmentant le risque d’exacerbations, d’hospitalisations, d’HTAP et de mortalité. Les micro-réveils répétés, la majoration du travail respiratoire nocturne et les désaturations favorisent l’inflammation systémique et l’instabilité respiratoire [10-14].
La présence d’un SAOS léger (IAH à 8/h), associé à une mauvaise efficacité du sommeil (50 %), à une somnolence diurne importante et à une hypoxémie nocturne, participe probablement à la fréquence des exacerbations. Le chevauchement BPCO–SAOS (« overlap syndrome ») est reconnu comme un facteur de mauvais pronostic, augmentant le risque d’exacerbations, d’hospitalisations, d’HTAP et de mortalité. Les micro-réveils répétés, la majoration du travail respiratoire nocturne et les désaturations favorisent l’inflammation systémique et l’instabilité respiratoire.
Rôle de l’oxygénothérapie de longue durée
L’oxygénothérapie de longue durée (OLD), prescrite chez ce patient à 2 L/min en continu, est indiquée devant la dyspnée sévère (mMRC 4) et l’hypoxémie chronique suspectée. L’OLD a démontré son bénéfice sur la survie, la tolérance à l’effort et la qualité de vie chez les patients BPCO présentant une hypoxémie sévère persistante. Dans ce cas, les gaz du sang sous O₂ montrent une PaO₂ élevée (124 mmHg), suggérant un possible surdosage en oxygène, exposant au risque d’hypocapnie ou de troubles de la régulation ventilatoire à long terme.
L’hypoxémie nocturne persistante malgré l’oxygène à 1 L/min justifie une réévaluation des besoins réels en oxygène, idéalement par gazométrie artérielle à l’air ambiant et sous O₂, ainsi qu’une éventuelle association à une ventilation nocturne par PPC si le SAOS devient plus sévère.
Intérêt de la réhabilitation respiratoire
La réhabilitation respiratoire est une composante essentielle de la prise en charge des BPCO sévères. Elle permet d’améliorer la dyspnée, la tolérance à l’effort, la qualité de vie, et de réduire le nombre d’exacerbations et d’hospitalisations. Chez ce patient très symptomatique (CAT à 32), déconditionné à l’effort et probablement sarcopénique, la réhabilitation est fortement indiquée. Elle doit être multidisciplinaire, associant réentraînement à l’effort, éducation thérapeutique, prise en charge nutritionnelle et soutien psychologique [15-19].
Vaccination antigrippale et antipneumococcique
L’absence de donnée sur la vaccination antigrippale et antipneumococcique représente un facteur de risque majeur évitable. Ces vaccinations sont formellement recommandées chez tous les patients BPCO, particulièrement chez ceux présentant des formes sévères et des exacerbations récurrentes. Elles réduisent significativement le risque d’infections respiratoires graves, d’exacerbations et de mortalité. La mise à jour du statut vaccinal constitue donc une priorité dans la prise en charge secondaire.
CONCLUSION
Ce cas illustre la complexité de la prise en charge d’une BPCO sévère chez un patient ancien grand fumeur, présentant des exacerbations fréquentes, une dyspnée majeure et des comorbidités métaboliques. L’association probable d’un syndrome d’apnées du sommeil, responsable de troubles du sommeil, d’une hypoxémie nocturne et d’une somnolence diurne importante, contribue à l’instabilité clinique et au mauvais contrôle de la maladie. L’oxygénothérapie de longue durée, bien qu’indiquée, doit être régulièrement réévaluée afin d’éviter le surdosage et d’optimiser son efficacité. La réhabilitation respiratoire représente un pilier fondamental pour améliorer la tolérance à l’effort, réduire la fréquence des exacerbations et restaurer l’autonomie fonctionnelle. Enfin, la mise à jour du statut vaccinal contre la grippe et le pneumocoque constitue un levier essentiel de prévention secondaire, souvent négligé, mais indispensable pour réduire la morbi-mortalité liée aux infections respiratoires.
RÉFÉRENCES
| 1. Global Initiative for Chronic Obstructive Lung Disease (GOLD). GOLD 2026 Report: Global Strategy for the Diagnosis, Management, and Prevention of COPD. GOLD; 2026. Available from: https://goldcopd.org. |
| 2. Nguyen-Nhu, V., Nguyen, L. P., Duong-Quy, S., Le An, P., & Bui-Minh, T. Classification of chronic obstructive pulmonary disease as ABCD according to the GOLD 2011 and 2017 versions in patients at the University Medical Center in Ho Chi Minh City, Vietnam. Monaldi Archives for Chest Disease, 2024;94(2). |
| 3. Duong-Quy, S., Vo-Pham-Minh, T., Duong-Thi-Thanh, V., Craig, T., & Nguyen-Nhu, V. Clinical approaches to minimize readmissions of patients with COPD: a narrative review. Current Respiratory Medicine Reviews, 2023;19(1), 12-23. |
| 4. Duong-Quy S, Nguyen-Huu H, Hoang-Chau-Bao D, Tran-Duc S, Nguyen-Thi-Hong L, Nguyen-Duy T, Tang-Thi-Thao T, Phan C, Bui-Diem K, Vu-Tran-Thien Q, et al. Personalized Medicine and Obstructive Sleep Apnea. Journal of Personalized Medicine. 2022; 12(12):2034. |
| 5. Duong-Quy S, T. Tang-Thi-Thao, T. Nguyen-Duy, Thu Vo-Pham-Minh. Management of Asthma, Chronic Obstructive Pulmonary Disease (COPD) and Obstructive Sleep Apnea (OSA) at Outpatient Unit - ACOSOU. J Func Vent Pulm 2025;48(16):1-4. |
| 6. DUONG-QUY, S.; HUYNH-ANH, T.; SOYEZ, F. Etude des caractéristiques du syndrome d’apnées obstructives chez les patients atteints de BPCO. J Func Vent Pulm, 2013, 4.11: 1-52. |
| 7. Le, Bao Khac, and Minh Hoang. "Prevalence of obstructive sleep apnea in patients with chronic obstructive pulmonary disease in Vietnam." Sleep and Breathing 28.4 (2024): 1589-1595. |
| 8. Nguyen-Thi-Y N, Le Van B, Duong-Quy S. Obstructive Sleep Apnea (OSA) in patients with Chronic Obstructive Pulmonary Disease (COPD). J Func Vent Pulm 2020;34(11):1-5. |
| 9. Duc Nguyen-Hong, Nhi Nguyen-Thi-Y, Quy Duong-Minh, Nghia Dam-Trung, Bang Le-Van, Sy Duong-Quy. Diagnosis and management of obstructive sleep apnea in patients with chronic obstructive pulmonary disease. J Func Vent Pulm 2024;46(15):1-6. |
| 10. Nguyen-Thi-Hong L, Duong-Quy S. Obstructive Sleep Apnea Syndrome: The challenges in developing countries. J Func Vent Pulm 2016;22(7):1-2. |
| 11. Duong-Quy, S., Mai, K. D. T., Van, N. T., Bich, H. N. X., Hua-Huy, T., Chalumeau, F., ... & Martin, F. Study about the prevalence of the obstructive sleep apnoea syndrome in Vietnam. Revue des maladies respiratoires, 2018;35(1), 14-24. |
| 12. Duong-Quy S. Osa personalized treatment of obstructive sleep apnea. J Func Vent Pulm 2023;43(14):1 |
| 13. Baud D. Treatment of sleep apnea syndrome by positive pressure at night. J Func Vent Pulm 2014;05(14):18-24. |
| 14. Hua–Huy, T. "Syndrome d’apnées obstructives du sommeil (SAOS): sur le bon chemin du dépistage." (2014). |
| 15. Hua-Huy, T., and S. Duong-Quy. "Lung function testing in chronic obstructive pulmonary disease (COPD)." J Func Vent Pulm 4.12 (2013): 1-47. |
| 16. Marin JM, Soriano JB, Carrizo SJ, Boldova A, Celli BR. Outcomes in patients with chronic obstructive pulmonary disease and obstructive sleep apnea: the overlap syndrome. American Journal of Respiratory and Critical Care Medicine, 2010; 182 (3), 325-331. |
| 17. McNicholas WT. COPD–OSA Overlap Syndrome: Evolving Evidence Regarding Epidemiology, Clinical Consequences, and Management. Chest, 2017; 152 (6), 1318-1326. |
| 18. Chung F, Abdullah HR, Liao P. STOP-Bang Questionnaire: A Practical Approach to Screen for Obstructive Sleep Apnea. Chest, 2016; 149 (3), 631-638. |
| 19. Spruit MA, Singh SJ, Garvey C, ZuWallack R, Nici L, Rochester C, et al. An official American Thoracic Society/European Respiratory Society statement: key concepts and advances in pulmonary rehabilitation. American Journal of Respiratory and Critical Care Medicine, 2013; 188 (8), e13-e64. |
FIGURES - TABLES


RÉFÉRENCES
| 1. Global Initiative for Chronic Obstructive Lung Disease (GOLD). GOLD 2026 Report: Global Strategy for the Diagnosis, Management, and Prevention of COPD. GOLD; 2026. Available from: https://goldcopd.org. |
| 2. Nguyen-Nhu, V., Nguyen, L. P., Duong-Quy, S., Le An, P., & Bui-Minh, T. Classification of chronic obstructive pulmonary disease as ABCD according to the GOLD 2011 and 2017 versions in patients at the University Medical Center in Ho Chi Minh City, Vietnam. Monaldi Archives for Chest Disease, 2024;94(2). |
| 3. Duong-Quy, S., Vo-Pham-Minh, T., Duong-Thi-Thanh, V., Craig, T., & Nguyen-Nhu, V. Clinical approaches to minimize readmissions of patients with COPD: a narrative review. Current Respiratory Medicine Reviews, 2023;19(1), 12-23. |
| 4. Duong-Quy S, Nguyen-Huu H, Hoang-Chau-Bao D, Tran-Duc S, Nguyen-Thi-Hong L, Nguyen-Duy T, Tang-Thi-Thao T, Phan C, Bui-Diem K, Vu-Tran-Thien Q, et al. Personalized Medicine and Obstructive Sleep Apnea. Journal of Personalized Medicine. 2022; 12(12):2034. |
| 5. Duong-Quy S, T. Tang-Thi-Thao, T. Nguyen-Duy, Thu Vo-Pham-Minh. Management of Asthma, Chronic Obstructive Pulmonary Disease (COPD) and Obstructive Sleep Apnea (OSA) at Outpatient Unit - ACOSOU. J Func Vent Pulm 2025;48(16):1-4. |
| 6. DUONG-QUY, S.; HUYNH-ANH, T.; SOYEZ, F. Etude des caractéristiques du syndrome d’apnées obstructives chez les patients atteints de BPCO. J Func Vent Pulm, 2013, 4.11: 1-52. |
| 7. Le, Bao Khac, and Minh Hoang. "Prevalence of obstructive sleep apnea in patients with chronic obstructive pulmonary disease in Vietnam." Sleep and Breathing 28.4 (2024): 1589-1595. |
| 8. Nguyen-Thi-Y N, Le Van B, Duong-Quy S. Obstructive Sleep Apnea (OSA) in patients with Chronic Obstructive Pulmonary Disease (COPD). J Func Vent Pulm 2020;34(11):1-5. |
| 9. Duc Nguyen-Hong, Nhi Nguyen-Thi-Y, Quy Duong-Minh, Nghia Dam-Trung, Bang Le-Van, Sy Duong-Quy. Diagnosis and management of obstructive sleep apnea in patients with chronic obstructive pulmonary disease. J Func Vent Pulm 2024;46(15):1-6. |
| 10. Nguyen-Thi-Hong L, Duong-Quy S. Obstructive Sleep Apnea Syndrome: The challenges in developing countries. J Func Vent Pulm 2016;22(7):1-2. |
| 11. Duong-Quy, S., Mai, K. D. T., Van, N. T., Bich, H. N. X., Hua-Huy, T., Chalumeau, F., ... & Martin, F. Study about the prevalence of the obstructive sleep apnoea syndrome in Vietnam. Revue des maladies respiratoires, 2018;35(1), 14-24. |
| 12. Duong-Quy S. Osa personalized treatment of obstructive sleep apnea. J Func Vent Pulm 2023;43(14):1 |
| 13. Baud D. Treatment of sleep apnea syndrome by positive pressure at night. J Func Vent Pulm 2014;05(14):18-24. |
| 14. Hua–Huy, T. "Syndrome d’apnées obstructives du sommeil (SAOS): sur le bon chemin du dépistage." (2014). |
| 15. Hua-Huy, T., and S. Duong-Quy. "Lung function testing in chronic obstructive pulmonary disease (COPD)." J Func Vent Pulm 4.12 (2013): 1-47. |
| 16. Marin JM, Soriano JB, Carrizo SJ, Boldova A, Celli BR. Outcomes in patients with chronic obstructive pulmonary disease and obstructive sleep apnea: the overlap syndrome. American Journal of Respiratory and Critical Care Medicine, 2010; 182 (3), 325-331. |
| 17. McNicholas WT. COPD–OSA Overlap Syndrome: Evolving Evidence Regarding Epidemiology, Clinical Consequences, and Management. Chest, 2017; 152 (6), 1318-1326. |
| 18. Chung F, Abdullah HR, Liao P. STOP-Bang Questionnaire: A Practical Approach to Screen for Obstructive Sleep Apnea. Chest, 2016; 149 (3), 631-638. |
| 19. Spruit MA, Singh SJ, Garvey C, ZuWallack R, Nici L, Rochester C, et al. An official American Thoracic Society/European Respiratory Society statement: key concepts and advances in pulmonary rehabilitation. American Journal of Respiratory and Critical Care Medicine, 2013; 188 (8), e13-e64. |
ARTICLE INFO DOI:10.12699/jfvpulm.17.51.2026.79
Conflict of Interest
Non
Date of manuscript receiving
10/9/2025
Date of publication after correction
17/12/2025
Article citation
Iris Hadadji, Lucie Pellier, Julia Pessiglione, Georgia Gesseau, Tang-Thi-Thao Tram, Nguyen-Tuan Anh, Do Xuan Hai, Bui Thi Kim Chi, Cao Thi Hong Mai, Pham Vu Thanh, Nguyen Xuan Tao, Victoire de Lastours, Sy Duong-Quy. Severe COPD with frequent exacerbations and suspicion of overlap syndrome in a retired 64 years-old patient: A case report. J Fran Vent PulmS 2026;51(17):80-84